Actualmente TAK-003 se está evaluando en un programa de dos dosis, administradas con un intervalo de tres meses, en el ensayo pivotal de eficacia de fase 3 TIDES.2
- Vacuna candidata contra el dengue de Takeda, asociada con una menor incidencia de dengue en niños y adolescentes; nuevos datos provisionales de fase 2 a los 18 meses publicados en The Lancet Infectious Diseases
-
El ensayo evalúa la seguridad e inmunogenicidad de distintos programas de la vacuna candidata contra el dengue TAK-003 en niños y adolescentes de 2 a 17 años que viven en áreas en las que el dengue es endémico.1
-
Los niños y adolescentes que recibieron TAK-003 tuvieron un riesgo relativo de dengue sintomático de 0,29 (IC del 95 %: 0,13-0,72) comparados con niños y adolescentes del grupo de control con placebo.1
-
TAK-003 provocó respuestas de anticuerpos sostenidas contra los cuatro serotipos de virus del dengue, independientemente de la exposición previa al dengue y del programa de administración de dosis.1
(7/11/2017 – web) Osaka, Japón.- Takeda Pharmaceutical Company Limited [TSE: 4502], (“Takeda”) anunció hoy que los datos provenientes de un análisis provisional de 18 meses del ensayo de fase 2 DEN-204 en curso de su vacuna candidata tetravalente contra el dengue, TAK-003 (también designada como TDV), han sido publicados en The Lancet Infectious Diseases. Los resultados de este análisis provisional, una evaluación previamente planificada de los datos de un ensayo en curso, muestran que TAK-003 está asociada con una reducción de la incidencia del dengue en niños y adolescentes.1 Estos datos también se presentaron hoy en la reunión anual de la American Society of Tropical Medicine and Hygiene.3 Se requieren datos de fase 3 para confirmar estos hallazgos.
El ensayo de fase 2 DEN-204 está en curso y evalúa la seguridad e inmunogenicidad de TAK-003 en 1.794 niños y adolescentes de 2 a 17 años en áreas con dengue endémico (la República Dominicana, Panamá y las Filipinas). El objetivo principal del ensayo es evaluar los niveles de anticuerpos inducidos por la vacuna contra los cuatro tipos de virus del dengue después de distintos programas de vacunación.4 Los participantes en el ensayo recibieron o una dosis primaria de TAK-003, dos dosis primarias de TAK-003 administradas con tres meses de diferencia, una dosis primaria de TAK-003 seguida por una dosis de refuerzo un año después, o un placebo.1 La vigilancia febril y la evaluación de la seguridad e inmunogenicidad continuarán a través del período de 48 meses del ensayo.1
Estos resultados provisionales mostraron:1
-
En el conjunto de seguridad (el grupo de participantes que recibió al menos una dosis de TAK-003 o un placebo), los niños y adolescentes que recibieron TAK-003 tuvieron un riesgo relativo de dengue sintomático de 0,29 (IC del 95 %: 0,13-0,72) comparados con los niños y adolescentes del grupo de control con placebo. La incidencia del dengue fue un criterio de valoración secundario del análisis, previamente especificado.1
-
Se determinó que TAK-003 fue segura y bien tolerada en términos de reacciones locales solicitadas y de eventos adversos sistémicos, en relación con el grupo de control con placebo. Esto resulta coherente con datos de estudios anteriores de fase 1 y 2.1
-
La respuesta inmunitaria contra los cuatro serotipos del dengue fue duradera en todos los grupos vacunados, con niveles de anticuerpos que persistieron a través del periodo de 18 meses independientemente del cronograma de vacunación o la exposición previa al virus del dengue.1
-
Hubo diferencias limitadas en la media geométrica de los títulos (geometric mean titers, GMT) y las tasas de seropositividad entre quienes recibieron una dosis primaria y quienes recibieron dos dosis primarias con un intervalo de tres meses, independientemente del estado serológico. Sin embargo, un dato muy importante, en los participantes que eran seronegativos al inicio, la segunda dosis administrada el mes 3 mejoró la tasa de seropositividad tetravalente en el mes 6 a 86 %, comparada con 69 % en el grupo de una dosis.1 Una dosis de refuerzo en el mes 12 dio como resultado una tasa de seropositividad tetravalente del 100 % en el mes 13 en los participantes que eran seronegativos al inicio.1
Estos hallazgos confirman la selección de un régimen de dos dosis, administradas con un intervalo de tres meses, para el pivotal ensayo en curso de eficacia de fase 3 de Takeda. Este régimen logra rápidamente un índice elevado de respuesta a los cuatro serotipos de dengue, independientemente de la exposición previa al dengue.1
“Estamos observando un perfil de seguridad aceptable y respuestas de anticuerpos sostenidas a través de los 18 meses de este ensayo. Estos datos son un paso importante en el desarrollo de nuestra vacuna candidata contra el dengue,” declaró Derek Wallace, M.B.B.S, Director del Programa Global del Dengue en Takeda.1 “La reducida incidencia del dengue en niños y adolescentes que reciben TAK-003 es alentadora; no obstante, se requieren datos de nuestro ensayo de eficacia de fase 3, TIDES, para confirmar estos hallazgos.”1
TAK-003 está actualmente siendo evaluada en el estudio de eficacia de inmunización tetravalente contra el dengue (Tetravalent Immunization against Dengue Efficacy Study, TIDES), un ensayo de eficacia de fase 3 de gran escala que se lleva a cabo en ocho países con dengue endémico.2 TIDES se basará en DEN-204 y otros estudios anteriores para seguir evaluando la tolerabilidad, la seguridad y la inmunogenicidad de la vacuna contra los cuatro serotipos del dengue en distintos grupos de edad y para determinar si la vacuna ayuda a prevenir el dengue sintomático.2, 5, 6 Los datos de TIDES estarán disponibles a fines de 2018.2
Acerca del estudio DEN-204 de fase 2
El estudio DEN-204 de fase 2 es un ensayo aleatorizado, doble ciego, controlado con placebo, multicéntrico, diseñado para evaluar la seguridad y la inmunogenicidad de un programa de una o dos dosis de TAK-003 en 1.794 participantes sanos que viven en áreas con dengue endémico (la República Dominicana, Panamá y las Filipinas).7
Acerca de TAK-003
La vacuna candidata tetravalente contra el dengue de Takeda (TAK-003) se basa en el virus vivo atenuado serotipo 2 (DENV-2) que brinda la estructura genética para los cuatro virus de la vacuna.8 Datos de la fase 1 y 2 han respaldado el avance hacia el estudio de la fase 3, sugiriendo que TAK-003 es segura y bien tolerada en niños y adolescentes (no ocurrieron EAS relacionados con la vacuna y la reactogenicidad fue limitada) e indujo inmunogenicidad contra los cuatro serotipos de dengue, incluso en participantes seronegativos. 7, 9, 10, 11
Acerca del dengue
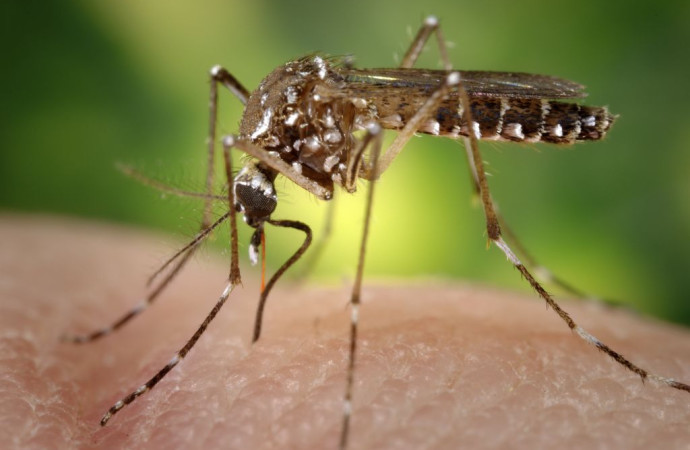
El dengue es la enfermedad viral más rápidamente transmitida por mosquitos.12 El dengue es difundido por los mosquitos Aedes aegypti y Aedes albopictus y es causado por cualquiera de los cuatro serotipos del dengue, cada uno de los cuales puede causar fiebre del dengue o dengue grave.13, 14 La prevalencia de los serotipos individuales varía ente diferentes geografías, países, regiones, estaciones y a lo largo del tiempo.15, 16
Se observan brotes de dengue en áreas tropicales y subtropicales y recientemente han causado brotes en partes de los EE. UU. continentales y Europa.13, 17, 18 Aproximadamente la mitad del mundo vive hoy en día bajo la amenaza del dengue, que es responsable de aproximadamente 390 millones de infecciones y 20.000 muertes en todo el mundo cada año.13, 19 El virus del dengue puede infectar a personas de todas las edades y es la causa principal de enfermedad grave en niños de algunos países de América Latina y Asia.13
Compromiso de Takeda con las vacunas
Las vacunas previenen más de dos millones de muertes cada año y han transformado la salud pública mundial.20 Durante 70 años, Takeda ha suministrado vacunas para proteger la salud de las personas en Japón. Actualmente, el negocio global de vacunas de Takeda aplica la innovación para afrontar algunas de las enfermedades infecciosas más desafiantes del mundo, como el dengue, Zika, norovirus y polio. Nuestro equipo posee una larga e impresionante trayectoria, así como vasto conocimiento en el ámbito de la creación de vacunas, fabricación y acceso global para proporcionar una serie de vacunas y, así, dar solución a algunos de los problemas de salud pública más urgentes que existen en el mundo.
El resumen del ensayo esta disponible en el siguiente enlace: Ensayo
Bibliografía
-
Sáez-Llorens, X., Tricou, V., et al. Immunogenicity and safety of one versus two doses of tetravalent dengue vaccine in healthy children aged 2–17 years in Asia and Latin America: 18-month interim data from a phase 2, randomised, placebo-controlled study. Lancet Infectious Diseases. 2017. Retrieved November 2017.
-
ClinicalTrials.gov. Efficacy, Safety and Immunogenicity of Takeda’s Tetravalent Dengue Vaccine (TDV) in Healthy Children (TIDES). 2017. Retrieved October 2017.
-
Wallace, D. et al. Progress in Development of Takeda’s Tetravalent Dengue Vaccine Candidate. 2017. Presented at 66th Annual Meeting, American Society of Tropical Medicine and Hygiene.
-
ClinicalTrials.gov. Safety and Immunogenicity of Different Schedules of Takeda’s Tetravalent Dengue Vaccine Candidate (TDV) in Healthy Participants. 2017. Retrieved October 2017.
-
ClinicalTrials.gov. A Comparison of the Safety and Immunogenicity of Various Schedules of Dengue Vaccine in Healthy Adult Volunteers. 2017. Retrieved October 2017.
-
ClinicalTrials.gov. Safety and Immunogenicity With Two Different Serotype 2 Potencies of Tetravalent Dengue Vaccine (TDV) in Adults in Singapore. 2017. Retrieved October 2017.
-
Sáez-Llorens, X., Tricou, V., et al. Safety and immunogenicity of one versus two doses of Takeda’s tetravalent dengue vaccine: Interim results of a long-term phase 2, randomized, placebo-controlled pediatric trial in Asia and Latin America. The Lancet Infectious Diseases. 2017. Retrieved October 2017.
-
Huang, C. Y.-H., et al. Genetic and Phenotypic Characterization of Manufacturing Seeds for Tetravalent Dengue Vaccine (DENVax). PLoS Neglected Tropical Diseases. 2013. Retrieved May 2016.
-
Osorio, J.E., et al. Safety and immunogenicity of a recombinant live attenuated tetravalent dengue vaccine (DENVax) in flavivirus-naive healthy adults in Colombia: a randomised, placebo-controlled, phase 1 study. The Lancet Infectious Diseases. 2014. Retrieved May 2016.
-
Wallace, D. Persistence of neutralizing antibodies one year after two doses of a candidate recombinant tetravalent dengue vaccine in subjects aged from 1.5 to 45 years. Presented at 6th Annual Meeting, American Society of Tropical Medicine and Hygiene. 2015.
-
Saez-Llorens, X., et al. Phase II, double-blind, controlled trial to assess the safety and immunogenicity of different schedules of Takeda’s Tetravalent Dengue Vaccine Candidate (TDV) in healthy subjects aged between 2 and <18 years and living in dengue endemic countries in Asia and Latin America. Presented at 5th Pan-American Dengue Research Network Meeting. 2016.
-
World Health Organization. Vector-borne diseases fact sheet. 2014. Retrieved August 2017.
-
World Health Organization. Dengue and Severe Dengue. 2016. Retrieved January 2017.
-
Centers for Disease Control and Prevention. Clinical Guidance Dengue Virus. 2014. Retrieved January 2017.
-
Bravo, L., et al. Epidemiology of Dengue Disease in the Philippines (2000-2011): A Systematic Literature Review. PLoS Neglected Tropical Diseases. 2014. Retrieved January 2017.
-
Guzman, M.G., et al. Dengue: a continuing global threat. Nature Reviews Microbiology. 2010. Retrieved May 2016.
-
Knowlton, K., et al. Mosquito-Borne Dengue Fever Threat Spreading in the Americas. The Natural Resources Defense Council (NRDC). 2009. Retrieved May 2016.
-
Chan E., et al. Using Web Search Query Data to Monitor Dengue Epidemics: A New Model for Neglected Tropical Disease Surveillance. PLoS Neglected Tropical Diseases. 2011. Retrieved January 2017.
-
Murray N.E., et. al. Epidemiology of dengue: past, present and future prospects. Clinical Epidemiology. 2013. Retrieved August 2017.
-
UNICEF. Immunization Facts and Figures. 2013. Retrieved January 2017.
Vía CCKCentroamerica




































Deja un comentario
Su dirección de correo electrónico no será publicada. Los campos requeridos estan marcados con *